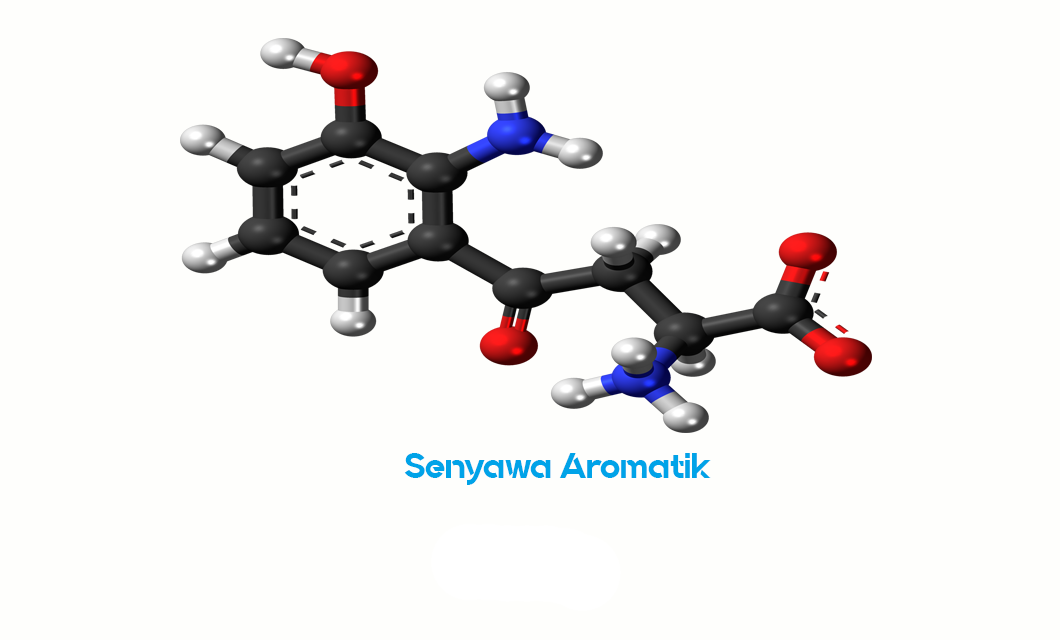
Senyawa aromatik merupakan senyawa organik yang mempunyai cincin aromatik, dengan terdiri dari atom karbon yang tersusun dalam rangkaian siklik khusus. Cincin aromatik ini mempunyai ikatan rangkap bergantian (ikatan pi), terdelokalisasi di sekitar cincin dan memberikan senyawa aromatik sifat khasnya.
Cincin aromatik pada senyawa aromatik paling terkenal, seperti benzena (C6H6), terdiri dari enam atom karbon terhubung oleh ikatan tunggal juga ikatan rangkap bergantian secara bergantian. Konfigurasi ini menghasilkan kestabilan energi lebih tinggi daripada apa yang diharapkan dari konfigurasi alternatif dengan ikatan tunggal juga ikatan rangkap tetap.
Aturan Huckel dikembangkan oleh fisikawan Jerman Erich Hückel untuk menjelaskan sifat-sifat khusus senyawa aromatik. Menurut aturan ini, suatu cincin aromatik dianggap aromatik jika jumlah elektron pi dalam cincin tersebut sama dengan 4n + 2, di mana n merupakan bilangan bulat non-negatif. Jumlah elektron pi ini biasanya berasal dari ikatan rangkap dalam cincin.
Senyawa aromatik mempunyai sifat-sifat khas, termasuk kestabilan, reaktivitas elektrofilik, juga kecenderungan untuk mengalami substitusi elektrofilik. Seyawa ini juga cenderung lebih tidak reaktif terhadap reaksi adisi sera lebih cenderung mengalami reaksi substitusi.
Contoh senyawa aromatik lainnya meliputi toluena, anilina, nitrobenzena, fenol, naftalena, juga banyak lagi. Masing-masing senyawa aromatik ini mempunyai gugus fungsional yang terikat pada cincin aromatik, memberikan karakteristik dan sifat khusus.
Senyawa aromatik digunakan dalam berbagai industri, termasuk industri kimia, farmasi, makanan dan minuman, parfum /kosmetik, tekstil, maupun bahan bakar. Senyawa ini juga digunakan dalam penelitian serta pengembangan ilmiah untuk sintesis senyawa baru dengan sifat-sifat khusus.
Penting untuk diingat bahwa tidak semua senyawa mempunyai aroma merupakan senyawa aromatik. Beberapa senyawa non-aromatik juga dapat mempunyai aroma kuat, sementara beberapa senyawa aromatik mungkin tidak mempunyai aroma yang terdeteksi oleh manusia. Identifikasi senyawa aromatik biasanya didasarkan pada struktur molekul juga sifat kimianya, bukan hanya pada aroma terkait.
Sejarah Senyawa Aromatik
Sejarah senyawa aromatik dimulai dengan penemuan senyawa benzena pada abad ke-19. Berikut ini merupakan gambaran umum tentang sejarah senyawa aromatik:
- Penemuan Senyawa Benzena: Pada tahun 1825, seorang ahli kimia Inggris bernama Michael Faraday mengisolasi senyawa benzena dari minyak karbon. Namun, struktur sebenarnya dari benzena masih belum diketahui pada saat itu.
- Perumusan Struktur Benzena: Pada tahun 1865, ahli kimia Jerman bernama Friedrich August Kekulé mengusulkan struktur benzena yang revolusioner. Ia menyatakan bahwa benzena mempunyai cincin yang terdiri dari enam atom karbon dengan ikatan rangkap bergantian dan ikatan tunggal. Ini dikenal sebagai struktur cincin Kekulé dan memainkan peran penting dalam perkembangan pemahaman tentang senyawa aromatik.
- Pengembangan Teori Aromatisitas: Pada awal abad ke-20, fisikawan Jerman bernama Erich Hückel memperkenalkan teori aromatisitas. Teori ini menjelaskan sifat khas senyawa aromatik berdasarkan jumlah elektron pi yang terlibat dalam cincin aromatik. Menurut aturan Hückel, untuk suatu cincin aromatik menjadi aromatik, jumlah elektron pi harus sama dengan 4n + 2, di mana n merupakan bilangan bulat.
- Penemuan Senyawa Aromatik Lainnya: Setelah penemuan benzena, para ilmuwan mulai menyintesis dan mengidentifikasi senyawa aromatik lainnya. Contohnya, pada tahun 1843, senyawa naftalena pertama kali diisolasi dari minyak batu bara. Kemudian, pada tahun 1856, senyawa toluena ditemukan sebagai turunan benzena.
- Pengembangan Ilmu Kimia Organik: Seiring berjalannya waktu, pemahaman tentang senyawa aromatik semakin berkembang dalam konteks ilmu kimia organik. Ahli kimia terus menyelidiki sifat dan reaktivitas senyawa aromatik, serta mengembangkan metode sintesis yang lebih efisien untuk memperoleh senyawa aromatik.
Sejak penemuan benzena dan perumusan struktur cincin Kekulé, senyawa aromatik telah menjadi subjek penelitian yang luas dalam bidang kimia organik. Penemuan dan pemahaman tentang senyawa aromatik telah memberikan dasar yang kuat bagi pengembangan industri kimia dan aplikasi yang beragam dalam berbagai bidang.
Sifat Senyawa Aromatik
Senyawa aromatik mempunyai sifat-sifat khas yang membedakannya dari senyawa non-aromatik. Berikut merupakan beberapa sifat umum dari senyawa aromatik:
- Kestabilan: Senyawa aromatik cenderung mempunyai kestabilan yang tinggi. Hal ini disebabkan oleh delokalisasi elektron pi di sekitar cincin aromatik, yang menghasilkan energi yang lebih rendah dibandingkan dengan senyawa non-aromatik yang mempunyai ikatan pi terlokalisasi. Kestabilan ini menyebabkan senyawa aromatik mempunyai kecenderungan untuk tetap dalam bentuk cincin aromatik yang tidak mudah mengalami reaksi kimia.
- Reaktivitas elektrofilik: Meskipun senyawa aromatik mempunyai kestabilan yang tinggi, mereka juga dapat mengalami reaksi kimia, terutama substitusi elektrofilik. Reaksi substitusi elektrofilik terjadi ketika gugus elektrofilik menyerang cincin aromatik dan menggantikan satu atom hidrogen dalam cincin. Hal ini disebabkan oleh keberadaan elektron pi yang tersedia di sekitar cincin aromatik.
- Reaktivitas adisi rendah: Salah satu sifat khas senyawa aromatik merupakan reaktivitas adisi yang rendah. Senyawa aromatik tidak cenderung mengalami reaksi adisi seperti senyawa alkena non-aromatik. Ini karena kestabilan cincin aromatik tidak terjaga jika terjadi penambahan gugus pada cincin. Sebagai gantinya, senyawa aromatik cenderung mengalami reaksi substitusi elektrofilik.
- Kekuatan ikatan: Senyawa aromatik mempunyai ikatan pi (ikatan rangkap) yang terdelokalisasi di sekitar cincin aromatik. Ikatan pi terdelokalisasi ini memberikan kekuatan ikatan yang lebih tinggi dibandingkan dengan ikatan pi pada senyawa non-aromatik yang terlokalisasi pada atom-atom tertentu dalam molekul. Ini berkontribusi pada kestabilan struktur senyawa aromatik.
- Keberadaan hibridisasi sp2: Atom karbon dalam senyawa aromatik mengalami hibridisasi sp2, yang menghasilkan ikatan sigma (ikatan tunggal) dengan atom karbon tetangga dan satu orbital p yang terlibat dalam delokalisasi elektron pi di cincin aromatik. Hibridisasi sp2 ini juga memungkinkan atom karbon aromatik untuk membentuk ikatan dengan atom-atom lain di luar cincin.
- Aroma khas: Beberapa senyawa aromatik mempunyai aroma yang khas dan menyenangkan. Minyak esensial dan senyawa aroma sering kali mengandung senyawa aromatik yang memberikan aroma yang diinginkan, seperti vanila, lavender, kayu manis, maupun mawar.
- Konduktivitas listrik: Beberapa senyawa aromatik dapat mempunyai sifat konduktivitas listrik tergantung pada struktur molekul dan keberadaan gugus fungsional yang terikat
- Polaritas: Secara umum, senyawa aromatik mempunyai polaritas yang rendah. Hal ini disebabkan oleh struktur cincin aromatik yang simetris dan distribusi elektron pi yang terdelokalisasi. Sebagai hasilnya, senyawa aromatik cenderung tidak larut dalam pelarut polar seperti air, tetapi lebih larut dalam pelarut nonpolar seperti pelarut organik.
- Titik leleh dan titik didih: Senyawa aromatik umumnya mempunyai titik leleh dan titik didih yang lebih tinggi dibandingkan dengan senyawa alifatik dengan massa molekul yang serupa. Ini disebabkan oleh kekuatan ikatan pi yang lebih tinggi dan kestabilan yang lebih besar akibat delokalisasi elektron pi di cincin aromatik.
- Keasaman: Beberapa senyawa aromatik mempunyai sifat asam yang lemah. Misalnya, fenol (C6H5OH) dapat melepaskan ion hidroksida (OH-) dalam air, sehingga mempunyai sifat asam yang lemah. Hal ini disebabkan oleh adanya gugus hidroksil yang terikat pada cincin aromatik.
- Magnetisme: Senyawa aromatik dapat menunjukkan sifat magnetik karena adanya elektron pi yang terdelokalisasi di cincin aromatik. Namun, magnetisme ini biasanya sangat lemah dan tergantung pada jumlah elektron pi yang terdelokalisasi dalam molekul.
Sifat-sifat senyawa aromatik dapat bervariasi tergantung pada struktur molekul, gugus fungsional yang terikat, dan lingkungan kimia. Oleh karena itu, tidak semua senyawa aromatik akan menunjukkan semua sifat-sifat yang telah disebutkan di atas.
Manfaat Senyawa Aromatik
Senyawa aromatik mempunyai berbagai manfaat dan aplikasi yang luas dalam berbagai bidang. Berikut ini merupakan beberapa manfaat utama senyawa aromatik:
- Industri Kimia: Senyawa aromatik digunakan dalam industri kimia untuk produksi berbagai bahan kimia, seperti plastik, serat sintetis, bahan pewarna, bahan baku farmasi, bahan pelembut, dan pelarut organik. Contohnya, benzena digunakan sebagai bahan baku dalam produksi plastik, serat poliester, dan bahan kimia lainnya.
- Farmasi: Senyawa aromatik mempunyai peran penting dalam industri farmasi. Banyak senyawa aromatik digunakan dalam sintesis obat-obatan, termasuk antibiotik, antidepresan, antikanker, analgesik, dan banyak lagi. Struktur aromatik sering kali memberikan aktivitas biologis yang diinginkan dalam molekul obat.
- Aromaterapi: Beberapa senyawa aromatik, seperti minyak esensial, digunakan dalam aromaterapi untuk tujuan relaksasi, pengobatan gangguan tidur, mengurangi stres, meningkatkan suasana hati, dan merangsang sistem kekebalan tubuh. Senyawa aromatik ini dapat dihirup maupun digunakan dalam bentuk minyak pijat.
- Industri Makanan dan Minuman: Senyawa aromatik sering digunakan sebagai bahan tambahan dalam industri makanan dan minuman untuk memberikan aroma dan rasa yang diinginkan. Misalnya, senyawa vanilin digunakan sebagai pemanis dan aroma vanila dalam makanan dan minuman.
- Parfum dan Kosmetik: Senyawa aromatik digunakan dalam pembuatan parfum, kosmetik, dan produk perawatan pribadi lainnya. Mereka memberikan aroma yang khas dan diinginkan dalam produk-produk tersebut.
- Tekstil: Beberapa senyawa aromatik digunakan dalam industri tekstil untuk pewarnaan serat maupun kain. Senyawa seperti anilina digunakan dalam produksi pewarna sintetis untuk memberikan warna yang tahan lama dan intens pada serat tekstil.
- Bahan Bakar: Senyawa aromatik, seperti bahan bakar minyak maupun bensin, juga digunakan sebagai sumber energi dalam industri dan transportasi.
Senyawa aromatik mempunyai banyak manfaat dan aplikasi lainnya tergantung pada jenis senyawa dan kebutuhan industri maupun sektor yang terkait. Penting untuk memperhatikan penggunaan yang tepat dan aman dari senyawa aromatik, karena beberapa di antaranya dapat bersifat toksik maupun berbahaya jika tidak ditangani dengan benar.
Contoh Senyawa Aromatik
Senyawa aromatik merupakan senyawa organik yang mempunyai ciri khas berupa cincin aromatik. Cincin aromatik terdiri dari atom karbon yang tersusun dalam rangkaian siklik yang memenuhi kriteria tertentu yang disebut dengan aturan Huckel. Salah satu contoh senyawa aromatik yang paling terkenal merupakan benzena (C6H6), yang mempunyai cincin aromatik yang terdiri dari enam atom karbon dengan ikatan tunggal dan ikatan rangkap bergantian.
Berikut ini merupakan beberapa contoh senyawa aromatik beserta rumus molekul dan nama umumnya:
| Senyawa Aromatik | Rumus Molekul | Nama Umum |
|---|---|---|
| Benzena | C6H6 | Benzena |
| Toluena | C7H8 | Toluena |
| Anilina | C6H5NH2 | Anilina |
| Nitrobenzena | C6H5NO2 | Nitrobenzena |
| Fenol | C6H5OH | Fenol |
| Naftalena | C10H8 | Naftalena |
| Antrasena | C14H10 | Antrasena |
| Pirena | C16H10 | Pirena |
| Indol | C8H7N | Indol |
| Antrakinon | C14H8O2 | Antrakinon |
Tabel di atas hanya memberikan contoh-contoh senyawa aromatik yang umum, dan masih banyak lagi senyawa aromatik lainnya dengan berbagai struktur dan gugus fungsional yang berbeda.
Berikut ini merupakan penjelasan singkat tentang masing-masing senyawa aromatik dalam tabel:
- Benzena (C6H6): Benzena merupakan senyawa aromatik yang paling sederhana. Molekulnya terdiri dari cincin aromatik enam atom karbon yang terhubung oleh ikatan tunggal dan ikatan rangkap bergantian. Benzena digunakan sebagai pelarut, bahan baku industri kimia, dan sebagai komponen dalam produksi plastik, serat, dan bahan kimia lainnya.
- Toluena (C7H8): Toluena merupakan senyawa aromatik dengan satu gugus metil (CH3) yang terikat pada cincin benzena. Ia sering digunakan sebagai pelarut, bahan baku dalam produksi bahan kimia, dan dalam sintesis obat-obatan dan bahan kimia lainnya.
- Anilina (C6H5NH2): Anilina merupakan senyawa aromatik yang mempunyai gugus amina (NH2) terikat pada cincin benzena. Ia digunakan dalam industri farmasi, produksi pewarna, dan sebagai bahan baku dalam pembuatan bahan kimia lainnya.
- Nitrobenzena (C6H5NO2): Nitrobenzena merupakan senyawa aromatik dengan gugus nitro (NO2) yang terikat pada cincin benzena. Ia digunakan dalam industri kimia sebagai bahan baku dalam produksi bahan peledak, bahan kimia organik, dan dalam sintesis obat-obatan dan bahan kimia lainnya.
- Fenol (C6H5OH): Fenol merupakan senyawa aromatik yang mempunyai gugus hidroksil (OH) yang terikat pada cincin benzena. Ia digunakan dalam industri farmasi, pembuatan resin, bahan kimia organik, dan dalam produksi bahan peledak.
- Naftalena (C10H8): Naftalena merupakan senyawa aromatik yang terdiri dari dua cincin benzena yang terhubung. Ia digunakan dalam industri kimia, termasuk produksi plastik, pewarna, bahan pelembut, dan sebagai bahan bakar untuk lampu kapur.
- Antrasena (C14H10): Antrasena merupakan senyawa aromatik yang terdiri dari tiga cincin benzena yang terhubung. Ia digunakan dalam industri pewarna, produksi obat-obatan, dan sebagai bahan baku dalam sintesis senyawa organik kompleks.
- Pirena (C16H10): Pirena merupakan senyawa aromatik yang terdiri dari empat cincin benzena yang terhubung. Ia termasuk dalam kelompok senyawa polisiklik aromatik dan sering digunakan dalam penelitian ilmiah dan aplikasi industri, seperti dalam produksi pewarna dan sebagai bahan aktif dalam peralatan optik.
- Indol (C8H7N): Indol merupakan senyawa aromatik yang terdiri dari cincin benzena yang terhubung dengan cincin azol (berisi nitrogen). Ia digunakan dalam industri farmasi untuk sintesis obat-obatan dan dalam penelitian
- Antrakinon (C14H8O2): Antrakinon merupakan senyawa aromatik yang mempunyai gugus keton (C=O) pada cincin benzena. Senyawa ini digunakan dalam industri pewarna, produksi obat-obatan, dan sebagai bahan kimia dalam sintesis senyawa organik kompleks.
Setiap senyawa aromatik dalam tabel mempunyai struktur molekul yang khas dan sifat-sifat kimia yang berbeda. Mereka digunakan dalam berbagai industri dan aplikasi, termasuk industri kimia, farmasi, pewarna, dan bahan kimia lainnya. Selain itu, senyawa aromatik juga menjadi bahan penelitian dalam ilmu kimia dan bio-kimia untuk memahami sifat dan reaktivitas senyawa organik.
Penting untuk dicatat bahwa sifat-sifat dan penggunaan senyawa aromatik dapat sangat bervariasi tergantung pada struktur molekul, gugus fungsional yang terikat, dan lingkungan penggunaan. Selain itu, keselamatan dan penanganan yang tepat harus dipertimbangkan ketika menggunakan senyawa aromatik, karena beberapa di antaranya dapat bersifat beracun maupun berbahaya jika tidak ditangani dengan benar.
Referensi
Berikut merupakan beberapa referensi yang dapat digunakan untuk mempelajari lebih lanjut tentang senyawa aromatik:
- Clayden, J., Greeves, N., Warren, S., dan Wothers, P. (2012). Organic Chemistry. Oxford University Press.
- Morrison, R. T., dan Boyd, R. N. (2007). Organic Chemistry. Prentice Hall.
- Silverstein, R. M., Webster, F. X., dan Kiemle, D. J. (2005). Spectrometric Identification of Organic Compounds. John Wiley dan Sons.
- Carey, F. A., dan Giuliano, R. M. (2018). Organic Chemistry. McGraw-Hill Education.
- Solomons, T. W. G., Fryhle, C. B., dan Snyder, S. A. (2017). Organic Chemistry. John Wiley dan Sons.
Selain itu, publikasi ilmiah, jurnal kimia, dan situs web sumber daya kimia dapat menjadi sumber informasi yang berguna tentang senyawa aromatik dan sifat-sifatnya.